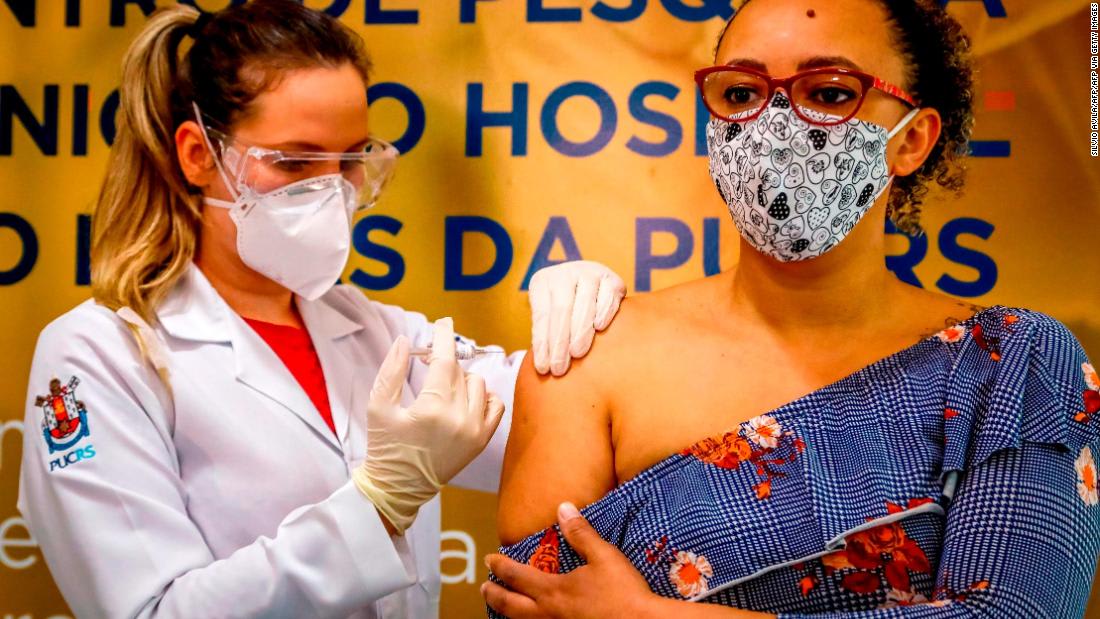
دبي، الإمارات العربية المتحدة (CNN)-- أوقفت الجهة المنظمة للصحة في البرازيل تجارب لقاح "كوفيد-19"، الذي طورته الصين، بعد "حالة ضارة وخطيرة" شملت متطوعًا.
وبدأت شركة الأدوية الصينية "سينوفاك بيوتيك" تجارب المرحلة الثالثة للقاح "CoronaVac"، بالتعاون مع معهد "بوتانتان" البرازيلي بمدينة ساو باولو، في أواخر يوليو/ تموز، بهدف ضم 130 ألف متطوع.
وتمثل تجارب المرحلة الثالثة مرحلة الاختبار النهائية والأكثر أهمية، قبل طلب الموافقة من الجهات المختصة.
ويعد هذا التوقف انتكاسة محتملة لأحد اللقاحات الرائدة في الصين. ويأتي ذلك في الوقت الذي قالت فيه شركة الأدوية الأمريكية "فايزر"، يوم الإثنين، إن البيانات المبكرة من لقاح كورونا تظهر فاعلية تزيد عن نسبة 90٪.
ووفقاً لمذكرة من الوكالة الوطنية للمراقبة الصحية في البرازيل، تسبب الحادث، الذي تم الإبلاغ عنه في 29 أكتوبر/ تشرين الأول، إلى اتخاذ قرار بتعليق التجربة، من أجل تقييم البيانات والمخاطر بشكل أفضل.
وجاء في المذكرة التي نشرتها CNN Brasil في وقت متأخر من يوم الإثنين: "مع توقف الدراسة، لا يمكن تطعيم أي متطوع جديد".
ولم توضح المذكرة ماهية الحدث الخطير أو مكان وقوعه، مستشهدة بمخاوف تتعلق بالخصوصية.
وقال معهد "بوتانتان" إنه سيعقد مؤتمراً صحفياً صباح الثلاثاء بالتوقيت المحلي، وفقاً لـCNN Brasil.
وفي بيان نُشر على الإنترنت يوم الثلاثاء، قالت شركة "سينوفاك" إنها "واثقة من سلامة اللقاح"، دون إعطاء سبب لتعليق التطعيم المبلغ عنه.
وأضافت: "تواصلنا مع شريكنا البرازيلي، معهد بوتانتان، ويعتقد رئيس المعهد أن الحادث لا علاقة له باللقاح. وستُبقي سينوفاك على التواصل مع الجانب البرازيلي في هذا الشأن.. وسيستمر العمل المتعلق بأبحاثنا السريرية في البرازيل بما يتفق بدقة مع معايير GCP (الممارسة السريرية الجيدة)".
ولا يعد إيقاف تجربة سريرية مؤقتاً بالأمر غير المعتاد. وفي سبتمبر/ أيلول، أوقفت شركة الأدوية العملاقة "AstraZeneca" التجارب العالمية للقاح فيروس كورونا، بسبب مرض غير مبرر لدى أحد المتطوعين.
والشهر الماضي، وصف حاكم ساو باولو، جواو دوريا، لقاح "CoronaVac" بأنه الأفضل والأكثر أماناً من بين جميع اللقاحات التي تم اختبارها في البرازيل، بعد قول معهد بوتانتان إن اللقاح أثبت أنه آمن في تجربة شملت 9 آلاف متطوع، بحسب "رويترز".
وتجري شركة "سينوفاك" أيضاً تجارب المرحلة الثالثة في إندونيسيا وتركيا. ولم ترد "سينوفاك" فوراً على طلب CNN للحصول على مزيد من التعليقات.
في الشهر الماضي، أعلن المسؤولون الصينيون ومطورو اللقاحات أنه لم يتم ملاحظة أي آثار جانبية خطيرة أو الإبلاغ عنها في التجارب السريرية لأي لقاح سريع الإنتاج في الصين.
وتمتلك الصين حالياً أربعة لقاحات لفيروس كورونا في المرحلة الثالثة من التجارب السريرية، ومعظمها يتم في البلدان النامية في جميع أنحاء العالم.
وفي مؤتمر صحفي في 20 أكتوبر / تشرين الأول، قال مسؤول بوزارة التكنولوجيا الصينية، إن إجمالي 60 ألف مشارك تم حقنهم بأربعة لقاحات صينية في تجارب المرحلة الثالثة، ولم يتم الإبلاغ عن أي آثار ضارة خطيرة.
وخلال الحدث نفسه، قال المدير العام لشركة "سينوفاك"، جاو تشيانغ، إنه رغم اكتشاف بعض الآثار السلبية الخفيفة في تجارب المرحلة الثالثة، إلا أنه لم يتم الإبلاغ عن أي ردود فعل خطيرة في البرازيل، أو إندونيسيا، أو تركيا.
وأوضح أنه أنشأ المتعاونون في الدول الثلاث "نظاماً شاملاً للكشف عن الآثار الضارة".
وقد تسبب اللقاحات، مثل أي دواء آخر، بعض الآثار الجانبية، ولكن عادة ما تكون طفيفة وقصيرة الأجل، مثل الألم، والطفح الجلدي، والصداع، أو الحمى.
ومن غير الواضح ما إذا كان تعليق البرازيل لتجارب "سينوفاك" سيكون له أي تأثير على تجارب الشركة الجارية في إندونيسيا وتركيا.
والأسبوع الماضي، قالت إندونيسيا إنها تخطط لتطعيم 9 ملايين شخص بلقاح "CoronaVac" من شركة "سينوفاك" في الأسبوع الثالث من ديسمبر/ كانون الأول، وذلك بموجب موافقة ترخيص الاستخدام في حالات الطوارئ من هيئة تنظيم الأدوية في البلاد.
وتواصلت CNN مع السلطات الصحية الإندونيسية والتركية للتعليق في ضوء قرار إيقاف الاختبار مؤقتاً في البرازيل.
وفي الصين، قام صانعو الأدوية بإعطاء لقاحات تجريبية لعشرات الآلاف من الأشخاص منذ يوليو/ تموز، في إطار برنامج الاستخدامات الطارئة الذي وافقت عليه الحكومة، والذي يسمح باستخدام اللقاحات المرشحة على نطاق محدود، قبل أن تثبت سلامتها وفعاليتها بشكل كامل من خلال التجارب السريرية.
وتعد هذه الخطوة مثيرة للجدل، حيث يخشى بعض الخبراء من أن التعقب السريع لعملية الموافقة العادية يمكن أن يعرض المشاركين لآثار جانبية غير معروفة، كما أن صانعي الأدوية الصينيين يخاطرون بما يتعارض مع معايير الأخلاق والسلامة الدولية.