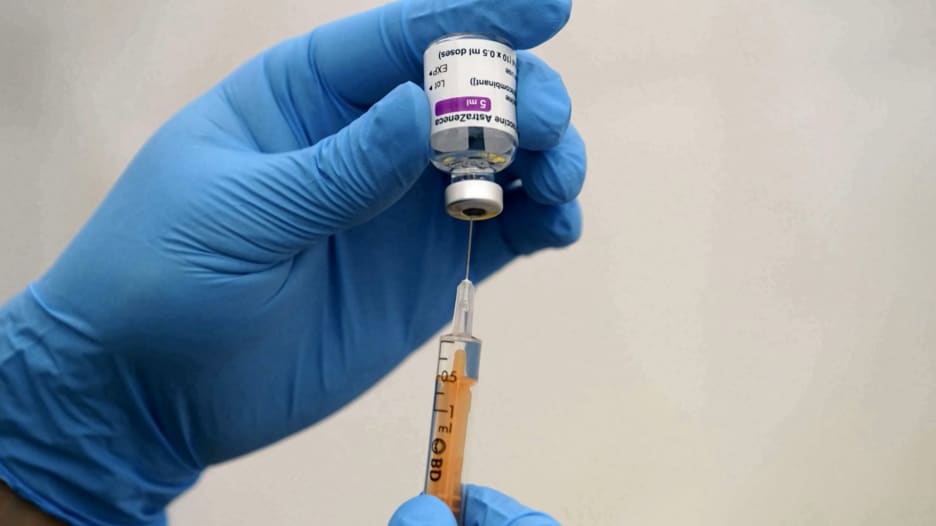
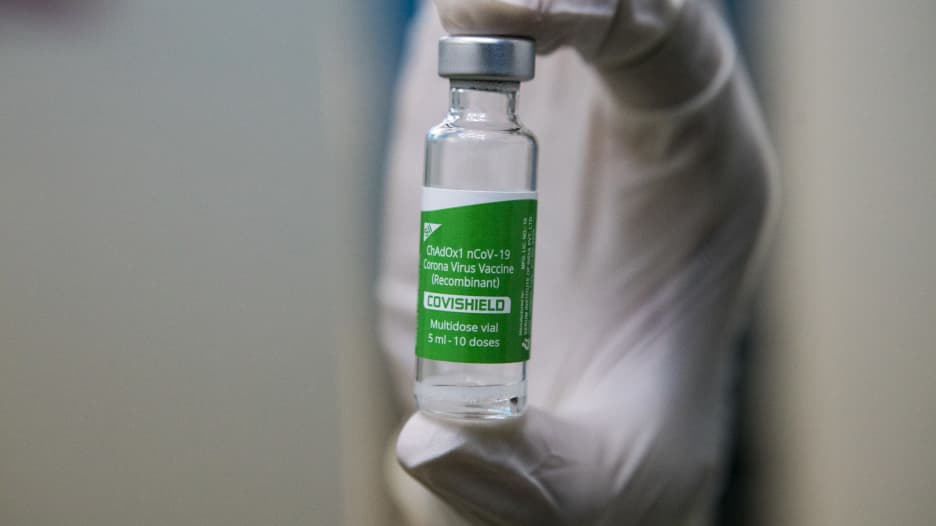
دبي، الإمارات العربية المتحدة (CNN) -- قامت شركة الأدوية العملاقة "أسترازينيكا" بتحديث بياناتها حول مدى كفاءة عمل لقاحها ضد فيروس كورونا.
وقالت "أسترازينيكا" في وقت متأخر من يوم الأربعاء إن اللقاح أظهر فعالية بنسبة 76% ضد مرض فيروس كورونا المصحوب بأعراض، وفعالية بنسبة 100% ضد الأمراض الشديدة أو الحرجة أو الحاجة إلى العلاج في المستشفى.
وأوضحت الشركة أن اللقاح كان فعالًا بنسبة 85% في منع أعراض المرض لدى المتطوعين الذين يبلغون من العمر 65 عاماً أو أكثر.
ولا تختلف الأرقام اختلافاً كبيراً عن البيانات التي أصدرتها الشركة في بيان يوم الاثنين.
وقامت الشركة بإصدار بياناتها عبر بيان صحفي وليس في تقرير راجعه النظراء أو كتقديم رسمي لمراجعة إدارة الغذاء والدواء الأمريكية.
وقال مين بانغالوس، نائب الرئيس التنفيذي لأبحاث المستحضرات الصيدلانية الحيوية في الشركة، ببيان: "يتوافق التحليل الأساسي مع تحليلنا المؤقت الذي تم إصداره سابقاً، ويؤكد أن لقاح كوفيد-19 الخاص بنا فعال للغاية لدى البالغين، بما في ذلك أولئك الذين تبلغ أعمارهم 65 عاماً وأكثر".
وأضاف بانغالوس: "نتطلع إلى تقديم طلبنا التنظيمي للحصول على ترخيص الاستخدام في حالات الطوارئ في الولايات المتحدة، والاستعداد لتوزيع ملايين الجرعات في جميع أنحاء أمريكا".
ويوم الثلاثاء، أعرب مجلس مراقبة البيانات والسلامة المستقل الذي يراجع بيانات العديد من لقاحات "كوفيد-19" عن قلقه بشأن إعلانات "أسترازينيكا" حول أحدث نتائجها. وعلى غير العادة، أعلن المعهد الوطني للحساسية والأمراض المعدية علناً عن هذه المخاوف.
وأشار المعهد الوطني للحساسية والأمراض المعدية، الذي ساعد شركة "أسترازينيكا" في إجراء تجارب اللقاح في الولايات المتحدة، إلى أن "مجلس مراقبة البيانات والسلامة أعرب عن قلقه من أن أسترازينيكا ربما أدرجت معلومات قديمة من تلك التجربة، والتي ربما قدمت رؤية غير كاملة لبيانات الفعالية".
وقال المعهد الوطني للحساسية والأمراض المعدية: "نحث الشركة على العمل مع مجلس مراقبة البيانات والسلامة لمراجعة بيانات الفعالية وضمان نشر بيانات الفعالية الأحدث والأكثر دقة في أسرع وقت ممكن".
وأشارت أسترازينيكا" يوم الإثنين إلى أن لقاح "كوفيد-19" الخاص بها أظهر فعالية بنسبة 79% ضد الأمراض المصحوبة بأعراض، وفعالية بنسبة 100% ضد الأمراض الشديدة والاستشفاء.
وأظهرت التجربة التي أجريت على 32،449 متطوعاً في الولايات المتحدة، وبيرو، وتشيلي أن الأشخاص الذين حصلوا على اللقاح كانوا أقل عرضة بنسبة 76% لأعراض فيروس كورونا، مقارنة بثلث المشاركين الذين حصلوا على الدواء الوهمي. ويتم إعطاء اللقاح على جرعتين، بفاصل أربعة أسابيع.
وكما هو الحال مع تجارب اللقاحات الأخرى، كانت الشركة تتطلع لمعرفة عدد الأشخاص الذين أصيبوا بأعراض "كوفيد-19" من الذين تلقوا التطعيم، مقارنة بالأشخاص الذين لم يتلقوا التطعيم.
وقالت الشركة: "كانت هناك 190 حالة في التحليل الأولي. وهناك 14 حالة إضافية محتملة يتم الفصل فيها، وبالتالي فإن العدد الإجمالي للحالات وتقدير النقاط قد يتقلب قليلاً".
وأضافت: "ستقدم أسترازينيكا أيضاً التحليل الأساسي للنشر المُراجع من قبل الأقران خلال الأسابيع المقبلة".
وكما هو الحال مع تجارب لقاح فيروس كورونا الأخرى، لم يتم فحص المتطوعين بانتظام للكشف عن فيروس كورونا، لذلك من غير المعروف عدد الأشخاص الذين أصيبوا بعدوى بدون أعراض.
وقالت الشركة: "أظهرت نقطة نهاية ثانوية رئيسية، أن الوقاية من الأمراض الشديدة أو الحرجة والاستشفاء، فعالة بنسبة 100%. وكانت هناك 8 حالات من كوفيد-19 شديدة لوحظت في التحليل الأولي مع كل تلك الحالات في مجموعة الدواء الوهمي".
وأضافت الشركة: "كان اللقاح جيد التحمل، ولم يتم تحديد مخاوف تتعلق بسلامة اللقاح".
ومن جانبه، وصف مدير المعهد الوطني للحساسية والأمراض المعدية الدكتور أنتوني فاوتشي في وقت سابق من هذا الأسبوع إصدار الشركة للبيانات المبكرة بأنه "خطأ غير مقصود"، وهو مصطلح رياضي يعني أنه كان خطأهم.
وقال فاوتشي إن البيانات "جيدة حقاً، لكن عندما وضعت في البيان الصحفي، لم تكن دقيقة تماماً".
وكافحت شركة "أسترازينيكا"، التي طورت اللقاح مع جامعة أكسفورد البريطانية، لقبول لقاحها.
وواجه تطوير "أسترازينيكا" للقاح العديد من التحديات، من أنباء عن إصابة اثنين من المتطوعين بأعراض عصبية في الخريف الماضي إلى توقف في طرح اللقاح في عدة دول أوروبية وسط مخاوف من تسببه في حدوث جلطات دموية.
وقالت وكالة الأدوية الأوروبية منذ ذلك الحين إنه لا يوجد دليل على أن اللقاح يمكن أن يسبب جلطات دموية.