دبي، الإمارات العربية المتحدة (CNN) -- أجمع مستشارو اللقاحات في إدارة الغذاء والدواء الأمريكية الأربعاء، على التصويت لصالح توسيع نطاق الاستخدام الطارئ للقاحي "مودرنا" و"فايزر بيو إن تيك" المضادين لـ"كوفيد-19" كي يشمل الأطفال الأصغر سنًا، بدءًا من عمر 6 أشهر.
وصوّت جميع أعضاء اللجنة الاستشارية للقاحات والمنتجات البيولوجية ذات الصلة، وعددهم 21، بـ"نعم" ردًا على السؤال التالي: "استنادًا إلى مجموع الأدلة العلمية المتاحة، هل فوائد لقاح "مودرنا" المضاد لكوفيد-19، عند إعطائه كسلسلة من جرعتين (25 ميكروغرامًا لكل جرعة)، تفوق مخاطر استخدامه لدى الرضع والأطفال بين 6 أشهر و5 سنوات"؟
كما صوّت الأعضاء بنعم على السؤال التالي: "استنادًا إلى مجموع الأدلة العلمية المتاحة، هل تفوق فوائد لقاح فايزر بيو إن تيك المضاد لكوفيد-19 عند إعطائه كسلسلة من 3 جرعات (3 ميكروغرامات لكل جرعة) مخاطر استخدامه لد الرضع والأطفال بين 6 أشهر و4 أعوام"؟
وستقرر إدارة الغذاء والدواء الأمريكية، التي تتّبع عادةً قرارات اللجنة، إذا كانت ستسمح باستخدام اللقاحين في حالات الطوارئ لدى الأطفال الصغار.
ورغم ذلك، لا يمكن إعطاء اللقاحين حتى يصوّت مستشارو اللقاحات لدى المراكز الأمريكية لمكافحة الأمراض والسيطرة عليها (CDC) على التوصية بهما، وتوافق عليها الدكتورة روشيل والينسكي، مديرة مراكز مكافحة الأمراض.
ومن المتوقع أن يصوت مستشارو اللقاحات في المراكز الأمريكية لمكافحة الأمراض والسيطرة على التوصية، السبت.
ويُعد الأطفال الذين تقل أعمارهم عن 5 أعوام، الفئة العمرية الوحيدة غير المؤهلة حاليًا لتلقي التطعيم ضد "كوفيد-19".
وسيصبح نحو 17 مليون طفل مؤهلين للحصول على لقاحات "كوفيد-19" ما أن يُعطى الترخيص لهذه الفئة العمرية.
من جانبها، قالت عضوة اللجنة الدكتورة أرشانا تشاترجي، عميدة كلية شيكاغو الطبية في جامعة روزاليند فرانكلين: "أن تكون قادرًا على التصويت للحصول على ترخيص للقاحين سيؤمنان حماية للأطفال بدءًا من 6 أشهر من هذا المرض الفتاك، فهذا أمر مهم للغاية".
وقارنت تشاترجي يوم التصويت مع اليوم الذي أُعلن فيه الترخيص لأولى لقاحات "كوفيد-19" للبالغين والمراهقين الأكبر سنًا، في ديسمبر/ كانون الأول، 2020.
الفوائد تفوق المخاطر بشكل واضح
وأوضحت عضوة اللجنة أوفيتا فولر، الأستاذة المشاركة بعلم الأحياء الدقيقة والمناعة في كلية الطب بجامعة ميتشيغان، عن لقاح "مودرنا"، أن "تبين لنا أنّ فوائده تفوق مخاطره بوضوح، لا سيما بالنسبة لأولئك الذين لديهم أطفال صغار يذهبون إلى الحضانات أو دور رعاية الأطفال الجماعية".
وأضاف عضو اللجنة، الدكتور آرت رينغولد، أنه رغم أن خطر الاستشفاء والوفاة الناجمة عن الإصابة بكوفيد-19 أقل لدى الأطفال الصغار مقارنة مع البالغين، فإن الأطفال يتلقون اللقاحات لحمايتهم من الأمراض ذات المخاطر المتدنية.
وتابع رينغولد، من جامعة كاليفورنيا في بيركلي: "إذا كان لدينا لقاح فوائده تفوق المخاطر، فإن إتاحته للناس يُعتبر خيارًا معقولاً".
وأشار الدكتور بيتر ماركس، المسؤول في إدارة الغذاء والدواء الأمريكية خلال اجتماع عُقد الأربعاء، إلى أن عدد حالات الاستشفاء والوفيات الناجمة عن "كوفيد-19" لدى الأطفال مثير للقلق، وهي أعلى بكثير مقارنة مع الوفيات وحالات الاستشفاء المرتبطة بالإنفلونزا.
ولفت إلى أن عدد وفيات بين الأطفال الذين يبلغون 4 أعوام أو أدنى، خلال العامين الأولين من انتشار الجائحة "يقارن بشكل رهيب مع ما شهدناه جراء الإنفلونزا في الماضي".
وتابع ماركس: "نحن نتعامل مع قضية تحتّم علينا توخي الحذر حتى لا نغفل عدد وفيات الأطفال، جراء عدد الوفيات الهائل المسجل بين كبار السن. فكل حياة مهمة"، مضيفًا أن "الوفيات التي يمكن الوقاية منها باللقاحات هي ما علينا القيام بشيء حيالها".
لقاح مودرنا "جيد التحمل" لدى الأطفال الصغار
وخلال اجتماع عقد الثلاثاء، صوّت مستشارو إدارة الغذاء والدواء بالإجماع لصالح توسيع نطاق تصريح الاستخدام الطارئ للقاح "مودرنا" ليشمل الأطفال الأكبر سنًا والمراهقين، الذين تتراوح أعمارهم بين 6 و17 عامًا، قائلين إنّ فوائده تفوق مخاطره.
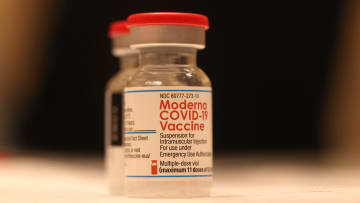
ووصفت الدكتورة ريتوبارنا داس، نائبة رئيس التطوير الإكلينيكي للقاحات "كوفيد-19"، خلال اجتماع الأربعاء، لقاح "مودرنا"، عند إعطائه بجرعة 25 ميكروغرام، بأنه "مقبول بشكل جيد" لدى الأطفال الذين تتراوح أعمارهم بين 6 أشهر و 5 سنوات.
وعن ردود الفعل السلبية، أوضحت داس أن الألم مكان الحقنة كان الأكثر شيوعًا، فضلًا عن الحراراة، والصداع، والتعب، وآلام العضلات، وآلام المفاصل، والغثيان، والقيء، والقشعريرة.
وبالنسبة للرضع، تضمنت ردود الفعل السلبية الحرارة، والتهيج، والبكاء، والنعاس، وفقدان الشهية.
وأوضحت داس أن ردود الفعل هذه كانت أكثر شيوعًا بعد تلقي الجرعة الثانية من اللقاح، وتلاشت خلال يومين أو ثلاثة أيام، مضيفة أن الحرارة كانت تقييمًا مهمًا لسلامة اللقاح لهذه الفئة العمرية.
وقالت داس لأعضاء اللجنة إن ارتفاع الحرارة بعد تلقي أي جرعة من اللقاح ظهر لدى نحو ربع الأطفال المشاركين، لكن غالبًا بعد تلقي الجرعة الثانية، واعتبرت حادثة واحدة من نوبات الحرارة مرتبطة بالتطعيم.
وبقي الطفل المصاب بالحرارة في دراسة اللقاح، وحصل على جرعة ثانية من اللقاح من دون تسجيل أي أحداث خطيرة.
وأكدت داس أنه لم يتم تسجيل أي وفيات، أو حالات التهاب بعضلة القلب، أو التهاب التامور بين متلقي اللقاح الصغار.
وأضافت: "باختصار، كان mRNA-1273 تقبله الأطفال بشكل جيد"، مستخدمًة الاسم التقني للقاح "مودرنا".
القلق بشأن عدد الجرعات
وقال عضو اللجنة، الدكتور بول أوفيت، خلال اجتماع الأربعاء، إن الأطفال الذين تلقوا لقاح "فايزر بيو ان تيك" يتعين عليهم إكمال سلسلة من ثلاث جرعات للحصول على الحماية الكافية.
وأوضح أوفيت، مدير مركز تعليم اللقاحات في مستشفى الأطفال بولاية بنسلفانيا، أنه رغم دعمه لحقيقة أن فوائد اللقاح تفوق مخاطره، إلا أن لديه بعض المخاوف بشأنه.
وبالمثل، أشارت عضو اللجنة، الدكتورة جانيت لي، من جامعة "أركنساس" للعلوم الطبية، إلى القلق من أن بعض الأطفال قد لا يكملون الجرعات الثلاث، وأن تلقي اللقاح سيكون بطيئًا.
وأضافت: "ما يقلقني هو ضرورة تلقي الجرعات الثلاث للحصول على الحماية المطلوبة".
وتضمنت بيانات المشاركين، المأخوذة من تجربة المرحلة 2/3 من لقاح فايزر، 1،678 طفل تلقوا جرعة ثالثة خلال الفترة التي سيطر فيها متحور أوميكرون من فيروس كورونا.
وتشير النتائج إلى أن اللقاح آمن وله استجابة مناعية قوية.
ولم تتم مراجعة البيانات أو نشرها في مجلة طبية.
وأعلنت شركتا "فايزر" و"بيو ان تيك" أن مستويات الأجسام المضادة، التي فُحصت بعد شهر من تلقي الجرعة الثالثة، أظهرت أن اللقاح أنتج استجابة مناعية مماثلة لتلقي جرعتين لدى الفئة العمرية بين 16 و25 عامًا.
في وثائق التقرير الصادر عن إدارة الغذاء والدواء الأمريكية، لوحظ أن بين الأطفال الصغار الذين تلقوا اللقاح خلال التجارب، لم تسجل حالات حساسية مفرطة، أو التهاب عضلة القلب، أو التهاب التامور.
وكانت ردود الفعل السلبية الأكثر شيوعًا بين الأطفال بين 6 أشهر و23 شهرًا التهيّج، والنعاس، وانخفاض الشهية، والألم في موقع الحقن.
بالنسبة للأطفال بين سنتين و4 أعوام، كانت ردود الفعل السلبية الأكثر شيوعًا التعب، والألم، والاحمرار في موقع الحقن.